
摘要
三维生物打印在癌症研究中受到了广泛的关注,其中迫切需要预测性和代表性肿瘤模型。这项研究调查了2D细胞培养和3D生物打印的肿瘤模型在评估乳腺癌和胰腺癌的侵袭性形式中的药效的用途。用顺铂和吉非替尼治疗2D和3D肿瘤模型,并比较细胞形态和细胞毒性的变化。顺铂和吉非替尼具有不重叠的作用 机制,分别干扰DNA修复机制和表皮生长因子受体(EGFR)信号传导。我们的发现验证了生物印制的类瘤是评估药物功效的可靠模型,并显示3D模型可实现相关的细胞形态和迁移模式,以及对抗癌药物的独特反应,而这些反应不同于传统的2D细胞培养系统。
介绍
在癌症生物学中,肿瘤微环境(TME)是肿瘤细胞与免疫系统之间的关键战区。TME是一整套细胞外基质(ECM),免疫细胞,信号分子,血管和成纤维细胞,可包裹肿瘤并影响癌症进展。TME的成分通过分 泌影响肿瘤行为各个方面的小信号分子而相互作用,这些分子包括细胞增殖,侵袭,转移和抗癌治疗的 耐药性(Bremnes,2011年)。 因此,重建TME对抗癌研究至关重要,但主要的挫折是无法开发用于高通 量药物评估的预测性3D肿瘤模型。 3D肿瘤模型应概述肿瘤基质中的细胞间相互作用,并克服2D细胞培养 系统的局限性。 在这里,3D生物打印为预测体内结果,对TME建模和评估药物反应提供了一种有前途的解决方案。
转移和化学耐药性威胁着癌症患者的生存。在癌症管理领域已显示出希望的一种治疗方式是化学疗法, 其使用小的抗癌分子攻击特定的生长途径并杀死癌细胞。此类分子中有顺铂(CIS)和吉非替尼(GEF) ,这是FDA批准的分别靶向DNA和EGFR途径的抗癌药物。简而言之,CIS通过抑制细胞分裂和mRNA的产生而导致凋亡,而GEF则干扰了癌细胞中EGFR信号的上调。有趣的是,虽然CIS和GEF都已用于治疗胰腺癌和乳 腺癌的致死形式,但它们在体外也与假阴性或假阳性预测相关联,表明它们在2D和3D中对细胞的影响不同(雷诺兹,2017)。为了进一步解决这一差异,我们比较了CIS和GEF对使用2种乳腺癌(MCF7,MDA MB 231)和2种胰腺癌(BxPC3,Panc-1)细胞系的2D单层和3D生物打印类瘤的影响。
材料和方法
细胞准备
从美国典型培养物保藏中心(ATCC)购买了两种胰腺癌细胞系(BxPC3,Panc-1)和两种乳腺癌细胞系 (MCF7,MDA MB 231)。 按照供应商的协议培养所有细胞系,每3至4天传代一次。 BxPC3细胞在带有L-谷氨 酰胺(Corning,参考号10-040-CV)的RPMI培养基中生长。 Panc-1细胞在含4.5g/L葡萄糖,L-谷氨酰胺和丙 酮酸钠(Corning,参考号10-013-CV)的DMEM中生长。MCF7细胞在EMEM(BD,Ref#670086)中培养; MDA和MDAMB 231细胞在不含L-谷氨酰胺(Corning,参考号10-045-CV)的无碳酸氢盐的Leibovitz L-15培养 基中生长。所有培养基均补充有10%FBS(Gibco,目录号16000044)和1%青霉素链霉素(Gibco,参考 号1509-70-063)。
生物墨水的制备和生物印刷
根据CELLINK规程准备了3mg/mL的Coll1(CELLINK,Ref#IK4000002001)和5%GelMA(CELLINK,Ref# IK3051020303)进行生物打印。将总共3 mL的Coll1或GelMA与5×106细胞/100μL培养基混合(10:1),并分别装入透明和琥珀色墨盒(CELLINK,Ref#CSO010311502),以?3kPa进行液滴打印。设置为8°C的温度控 制打印头(TCPH,SKU#000000020346)和气动打印头分别用于在8°C打印床上生物打印Coll1和 GelMA液 滴。使用BIOX(CELLINK,SKU#000000022222)上的液滴打印功能,将每种生物墨水打印在未经处理的96孔 板(Thermo Fisher Scientific,目录号267427)中。 印刷后,将Coll 1液滴在37°C下热交联20分钟,然 后将GelMA液滴在365nm下进行UV交联6秒钟。将100μL培养基添加到每个孔中,并每2至3天刷新一次。
2D单层培养
为了进行2D比较,将每种细胞系接种到经过处理的96孔板中(ThermoFisher Scientific,Cat#167425)。 培养48小时后, 针对每种细胞类型优化了细胞接种密度,以达到90%融合。 Panc-1细胞以1.2 x 104细胞/ 孔接种,BxPC3细胞以1.7 x 104细胞/孔接种,MCF7细胞以2.0 x 104细胞/孔接种,MDA MB 231细胞以2.0 x 104细胞/孔接种好。
药物治疗与分析
用不同浓度的吉非替尼(LC Laboratories,#G-4408)或顺铂(Cayman Chemical Company)分别将生物打 印的类瘤和2D单层膜分别处理96小时和48小时。使用MTS分析(Sigma-Aldrich)和LIVE/DEAD染色试剂盒 (Invitrogen)评估2D和3D条件下的细胞活力。 所有测定均按照制造商的说明进行。 使用EVOS Auto 2荧光 显微镜(Thermo Fisher Scientific)采集图像。
统计分析
使用GraphPad Prism 8.2.1进行统计分析。 所有数据均表示为六联体进行的两个实验的平均值±SEM。 使用 单向方差分析(ANOVA)分析治疗条件的差异,并认为p值<0.05显着。
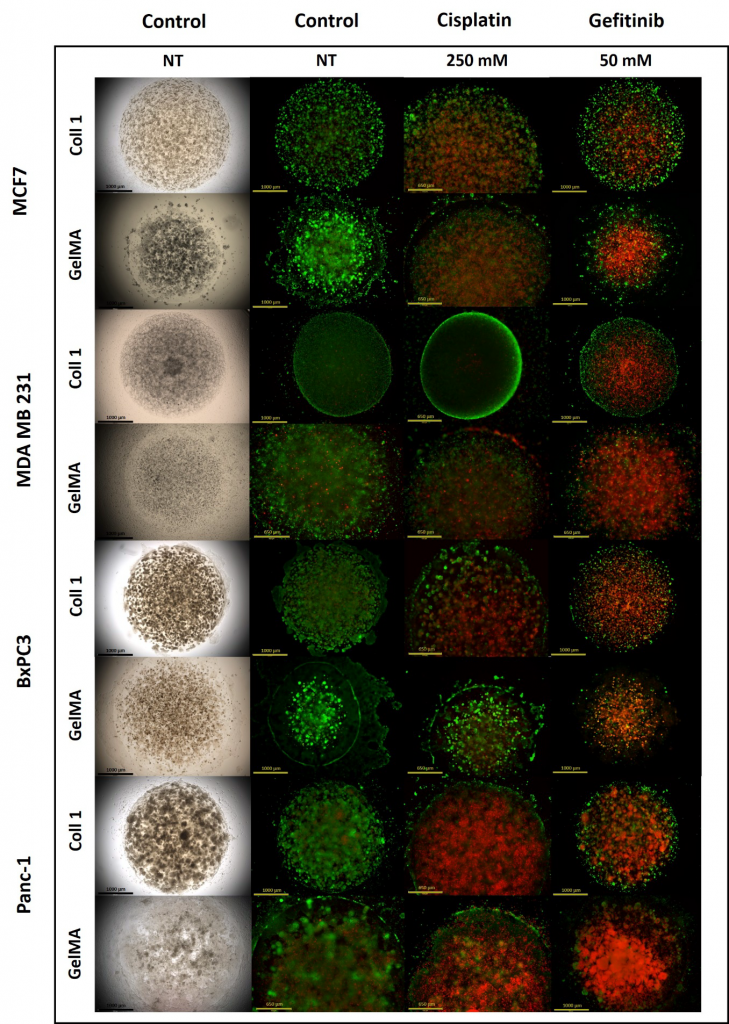
图 1. 在第11天,生物打印的类瘤的相衬度和LIVE / DEAD图像。优化了Calcein-PI分析以进行3D培养,并用于说明高浓度顺铂或吉 非替尼的细胞死亡。 该测定法的益处显示了抗肿瘤药对所有4种细胞系的强大作用,并描绘了每种细胞类型和ECM的细胞形态变化。 比例尺= 1000 μm或650 μm。 绿色=活着,红色=死了。
结果和讨论
生物打印类瘤中的球体形成和细胞形态
肿瘤会根据细胞类型和培养条件适应不同的形态(Nath,2016年)。 在GelMA和Coll 1中培养7天后,癌细 胞已经聚集形成各种形态的球体。 如图1所示,MDA MB 231细胞形成同心的星状网络,MCF7细胞形成圆形 的球体,BxPC3细胞形成葡萄状的椭圆体,而Panc-1细胞形成质量球体。 由于孔隙度,刚度和组成的差 异,将GelMA和Coll 1用作肿瘤支架也会影响球体的形成。 有趣的是,在2D培养物中生长的癌细胞缺乏所 描述的形态,可能是因为它们缺乏支持细胞间相互作用,紧密连接以及营养和氧气梯度的ECM(数据未显 示)。
缺氧3D模型中
缺氧是药物反应的另一个变量,对于3D模型和体内组织而言是唯一的。 Warburg效应将缺氧描述为癌细胞 的生存模式,在该模式中,缺氧从产生氧气和ATP转变为上调EGFR和AKT信号转导,从而促进增殖。 此开关 增加了3D模型中的毒性,酸性和废物堆积,从而创建了3环低氧梯度。 低氧梯度如图1所示,其中朝向球体 中心的细胞似乎是死的(红色),而边缘周围的细胞是可行的(绿色)。 由于废物堆积和缺氧,最外面的 环是一层增殖细胞,中间的环是一层活细胞,而最里面的环是坏死细胞的核心(Nath,2016年)。
顺铂在2D和3D中的功效
在第2天和第7天分别将低剂量至高剂量的CIS添加到2D单层和3D生物打印的类瘤中。 2D单层治疗持续48小 时,3D生物打印类瘤持续96小时。 MTS分析揭示了所有细胞系以及3D乳腺癌类肿瘤在2D单层中的剂量依赖 性细胞毒性(图2A)。 有趣的是,BxPC3和Panc-1细胞系在3D中显示的IC50高于2D。 换句话说,两种胰腺 癌细胞系在3D生物打印的类瘤中均不受CIS影响。 在这里,一种解释是胰腺癌细胞显示出对增加的CIS浓度 有抗性(Wang,2016; Kelland,2007; Sangster-Guity,2011)。 响应药物治疗,胰腺癌细胞可能已 经诱导了它们的生存途径,上调了衰老,DNA损伤反应信号和跨病变DNA的合成(Gomes,2019)。
吉非替尼在2D和3D中的功效
EGFR癌蛋白通常在乳腺癌和胰腺癌细胞系中过表达。 因此,药物对EGFR途径的抑制作用可导致细胞周期停滞,衰老或凋亡(Jacobi,2017)。 如图2B所示,吉非替尼在3D和2D中显着降低了细胞活力。 对于所有 细胞类型,3D Coll 1和GelMA的IC50均低于2D培养物的IC50,这表明GEF在3D生物打印类瘤中的死亡比2D培 养物中的死亡更多。
2D细胞培养系统的局限性
二维细胞培养系统无法模仿体内肿瘤的固有特性,包括天然屏障,低氧梯度和减缓药物扩散的紧密细胞间 连接。 此外,它们缺乏支持3D生长和癌蛋白上调的组织特异性环境和ECM(Reynolds,2017)。 再次查看 图2A,表明3D中的胰腺癌细胞比2D单层中生长的相同癌细胞对CIS的抵抗力更高。 在这里很明显,仅进 行2D研究对于体内胰腺癌的治疗会产生误导和不准确的预测。
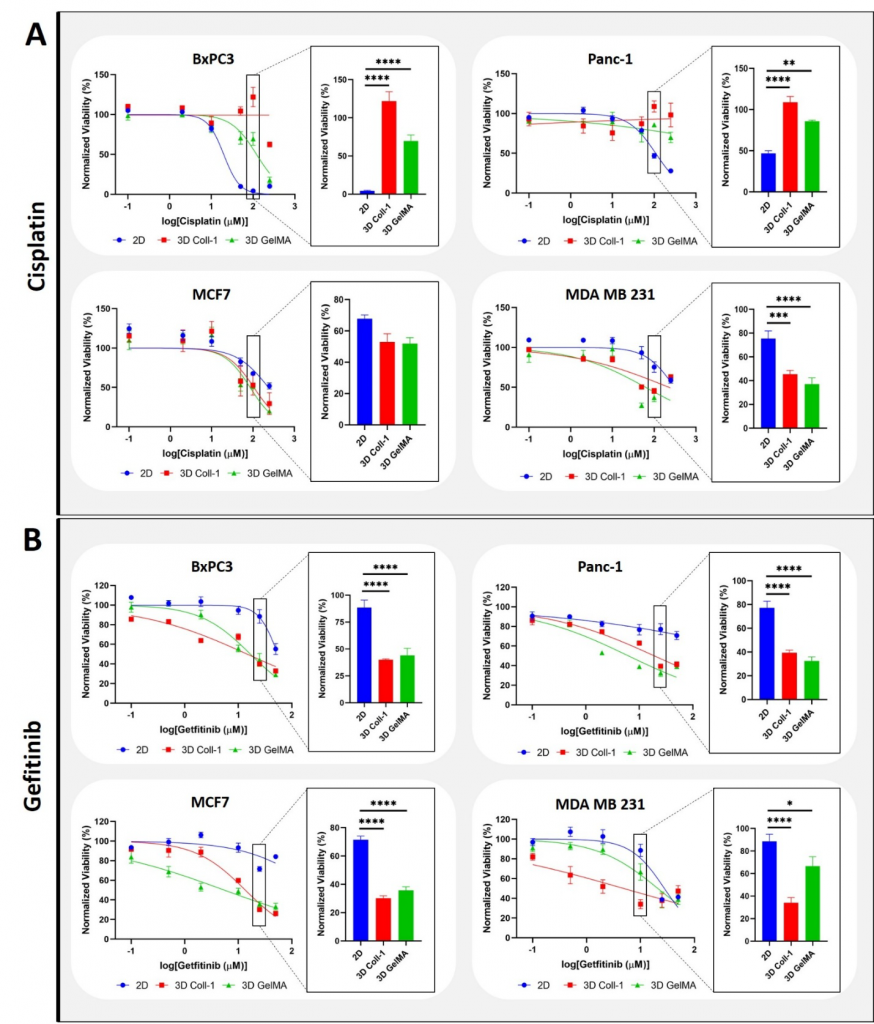
图 2. 顺铂(A)或吉非替尼(B)处理的乳腺癌细胞和胰腺癌细胞的剂量反应曲线。 使用代谢MTS测定法,相对于未处理的对照,确 定细胞活力。 数据读取为6次重复的平均值±SEM。
结论
*使用CELLINK GelMA和Coll 1作为类瘤的支架,可为球体形成和药物扩散提供稳定的TME。
*用GelMA和Coll 1制成的构建体的不同杀伤曲线模式表明,ECM在药物反应中起关键作用。将来需要进行研究以确定哪种支架适合特定的肿瘤模型。
*我们的发现表明,在2D和3D肿瘤模型中,对顺铂和吉非替尼治疗的剂量依赖性和细胞特异性反应。在3D模式下,乳腺癌和胰腺癌细胞系对GEF治疗的敏感性要高于2D模式。同样,乳腺癌细胞系 在3D中比2D对CIS治疗更敏感,但胰腺细胞系显示相反的作用,表明3D模型中耐药性水平升高。
*生物打印的类瘤是用于药物筛选的相关3D模型,可用于减少假阴性和假阳性预测的情况。未来的研究 可以使用BIO X扩大类瘤的生产,以进行高通量药物测试。
参考文献
1. Bremnes, R. M., D?nnem, T., Al-Saad, S., et al. The role of tumor stroma in cancer progression and prognosis: Emphasis on carcinoma-associated fibroblasts and non-small cell lung cancer. Journal of Thoracic Oncology. 2011; 6(1): 209-211. DOI:10.1097/JTO.0b013e3181f8a1bd.
2. Gomes, L. R., Rocha, C. R. R., Martins, D. J., et al. ATR mediates cisplatin resistance in 3D-cultured breast cancer cells via translesion DNA synthesis modulation. Cell Death and Disease. 2019; 10(6): 459. DOI: 10.1038/s41419-019-1689-8.
3. Jacobi, N., Seeboeck, R., Hofmann, E., et al. Organotypic three-dimensional cancer cell cultures mirror drug responses in vivo:Lessons learned from the inhibition of EGFR signaling. Oncotarget. 2017; 8(64): 107423-107440. DOI: 10.18632/oncotarget.22475.
4. Kelland, L. The resurgence of platinum-based cancer chemotherapy. Nature Reviews Cancer. 2007; 7: 573–584. DOI: 10.1038/nrc2167.
5. Nath, S., and Devi, G. R. Three-dimensional culture systems in cancer research: Focus on tumor spheroid model. Pharmacology and Therapeutics. 2016; 163: 94–108. DOI:10.1016/j.pharmthera.2016.03.013.
6. Reynolds, D. S., Tevis, K. M., Blessing, W. A., et al. Breast cancer spheroids reveal a differential cancer stem cell response to chemotherapeutic treatment. Scientific Reports. 2017; 7(1): 10382. DOI: 10.1038/s41598-017-10863-4.
7. Sangster-Guity, N., Conrad, B. H., Papadopoulos, N., et al. ATR mediates cisplatin resistance in a p53 genotype-specific manner. Oncogene. 2011; 30(22): 2526–2533. DOI: 10.1038/onc.2010.624.
8. Wang, S., Xie, J., Li, J., et al. Cisplatin suppresses the growth and proliferation of breast and cervical cancer cell lines by inhibiting integrin β5-mediated glycolysis. American Journal of Cancer Research. 2016; 6(5): 1108–1117. PMID: 27294003.

